ContenidosENZIMAS: material de apoyo al curso
¿qué es enzima?
definición
Catálsis nos lleva a ...
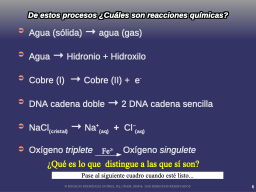
¿qué es reacción química?
Identifique las RXNs Químicas
Slide 7
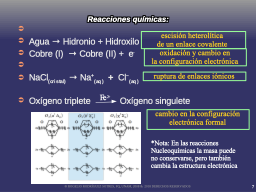
Reacciones_químicas
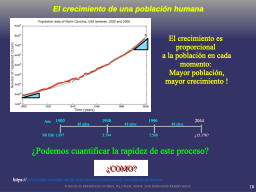
¿cómo medir la rapidez de RXN?
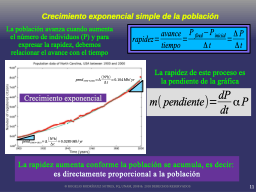
crecimiento exponencial
pendiente
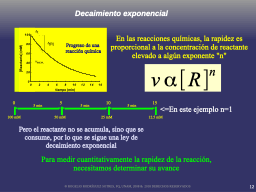
decaimiento expenencial
Ejemplo
¿cuántos valores de rapidez de RXN hay?
Definición de rapidez de RXN
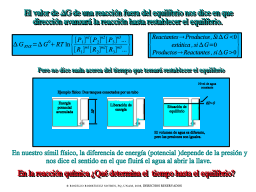
¿En qué sentido avanza una RXN química?
Identifique el sentido en estas RXNs
El sentido en que ocurren es ...
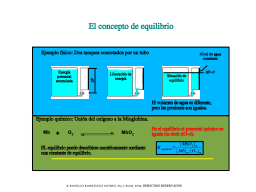
En concepto de equilibrio
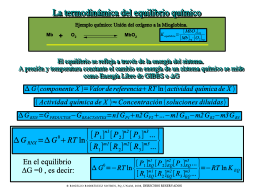
Constante de equilibrio y potencial químico
¿En cuánto tiempo se llega al equilibrio?
Concepto de parámetros de estado
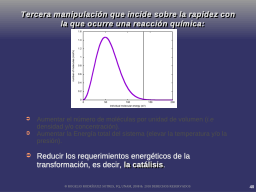
¿Qué hace a una reacción rápida o lenta?
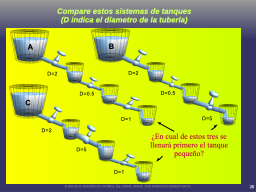
Identifique al más rápido...
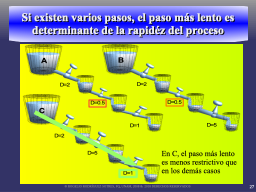
Proceso lento
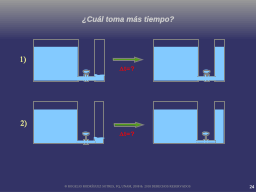
¿Cuál fluye más rapido?
...y qué pasa si ocurre en etapas
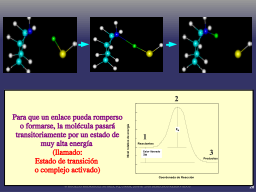
El concepto de estado de transición
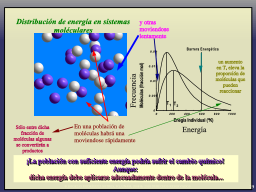
Energía y movimiento molecular
Relación de rapidez y número de moléculas
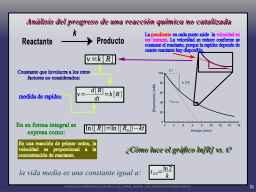
Modelado del progreso de una RXN Q
Otras relaciones de cinética química
¿Cómo identificar a los determinantes de la rapidez?
La cinética química requiere experimentos
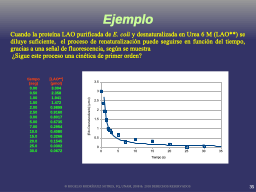
Ejemplo, desnaturalización de LAO
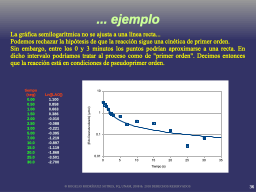
Desnaturalización LAO semilog
Resultado del ejemplo LAO
Rapidez y temperatura
Relación entre rapidez y temperatura
Rapidez y trayectoria hacia productos
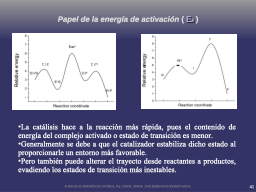
La coordenada de RXN con y sin E
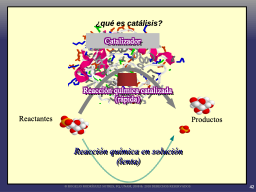
Definición de catálisis
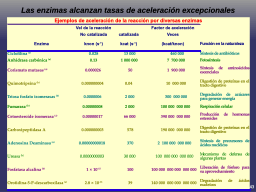
Datos del poder catalítico de las enzimas
Concluyendo: las enzimas intervienen la cinética de RXN
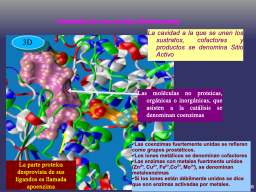
Anatomía de una enzima
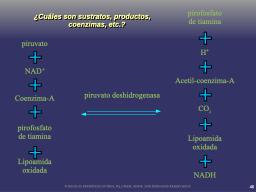
Ejemplo de coenzimas
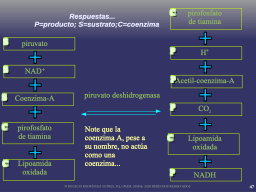
Ejemplo de coenzimas... respuestas
bases de la clasificación internacional EC
Un ejemplo y fuentes de información
EC 7.x.x.x
¿Qué características tiene una E?
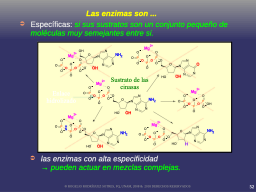
Especificidad
Baja especificidad vs. promiscuidad
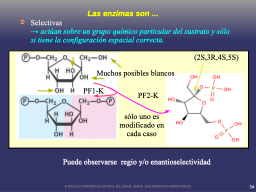
Selectividad
Ejemplo de enantioselectividad
Ejemplo de enantio y regioselectividad
Son eficientes y no se consumen en la RXN
Travajan en condiciones suaves
¿Cómo estudiarlas?
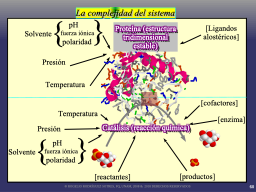
Dualidad: catalisis vs. estabilida de la enzima
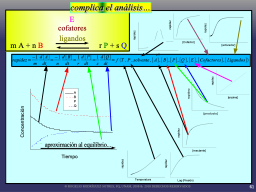
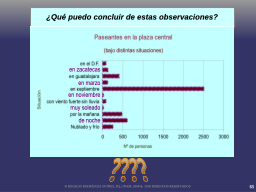
Las múltiples variables involucradas
Slide 62
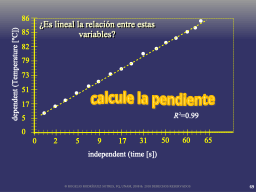
¿como mostrar la relación entre dos variables?
Slide 64
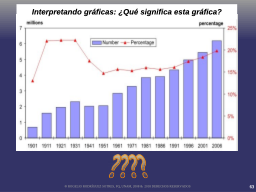
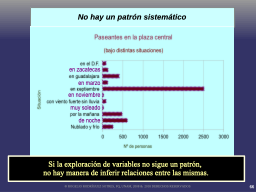
Esplorando las relaciones entre variables
Slide 66
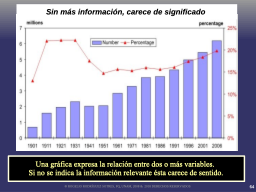
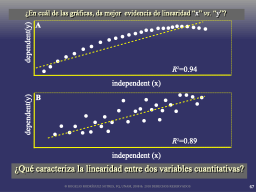
Relaciones lineales e incertidumbre estocástica
Slide 68
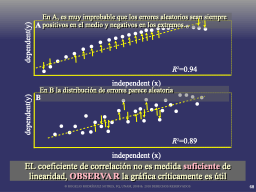
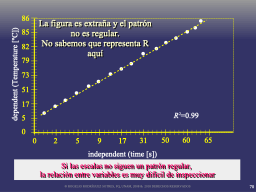
La escala de representación y la aparente linearidad
Slide 70
Recomendaciones al analizar resultados gráficos
Slide 72
Slide 73
Aspectos relevantes a considerar al medir
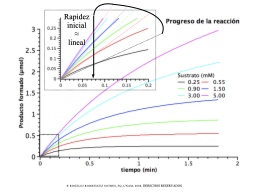
Una RXN enzimática: variando [S]
¿Qué pasa si varío [S] con [E] constante?
La rapidez si depende de [S]
Una RXN enzimática: variación en [E]
resultado de variar la enzima
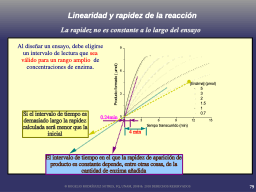
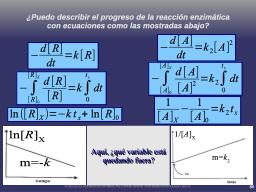
Ecuaciones típicas de la cinética química
Función esperada
Progreso a tiempos muy cortos
Progreso a tiempos más largos
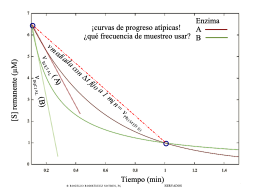
Sitauciones atípicas, inestabilidad de la E
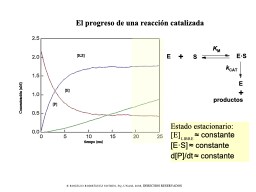
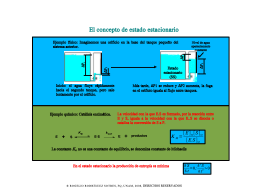
el concepto de estado estacionario (SS)
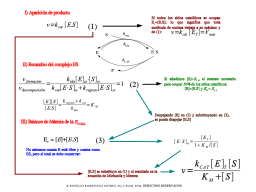
modelando una RXN enzimática en SS
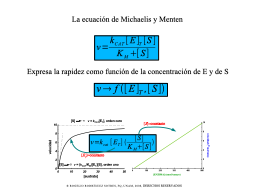
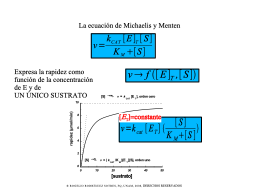
La expresión de Michaelis y Menten
Isoterma de saturación por el sustrato
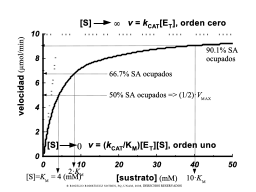
Caso extremo con [S] >> Km
Caso extremo con [S] << Km
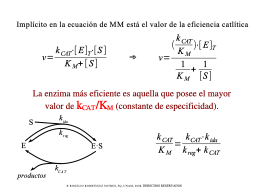
Interpretación de V/K
capacidad catalítica y afinidad combiandas
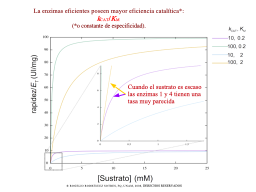
Importancia de la eficiencia catalítica en la célula
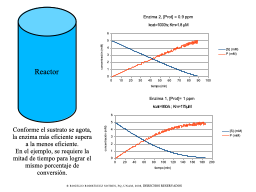
Importancia de kcat/Km en un reactor
V/K y límite de la difusión
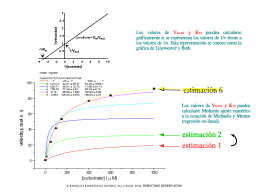
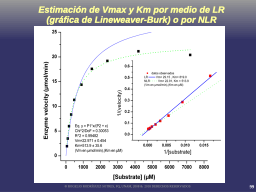
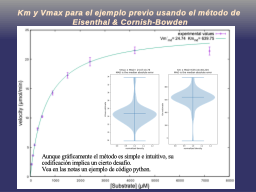
Cálculo de Km y Vmax
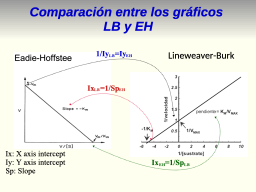
La grafica 1/V vs. 1/[S] e incertidumbre
Un ejemplo con números
Resultado gráfico
Slide 100
Slide 101
Slide 102
Slide 103
Slide 104
Slide 105
Enzimas multisustrato
La ecuación de Michaelis-Menten
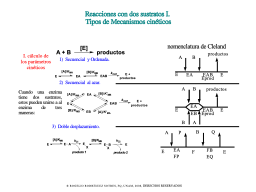
Tipos de mecanismos cinéticos (bisustrato)
Relación entre kcat y [E·S]
Relación entre V/K y [E]libre
Patrón de rapidéz inicial bisustrato
Patrón intersectante, reacciones secuenciales
Patrón paralelo, reacciones ping-pong
Inhibición por los productos
Identificando el orden: patrones de inhibición
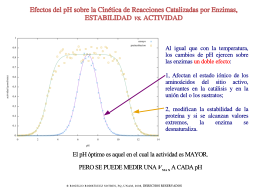
Cambios de pH en actividad enzimática
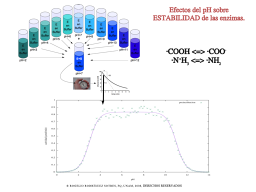
pH y actividad
pH y estabilidad
Disección de los efectos
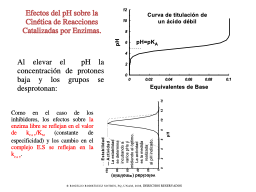
La inización del sitios activo
Efectos sobre [E]libre y [ES]
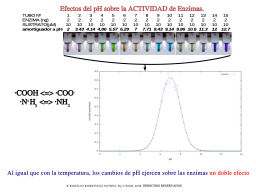
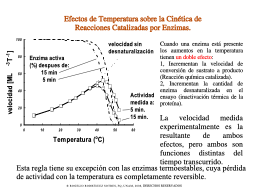
Efectos de Temperatura y actividad enzimática
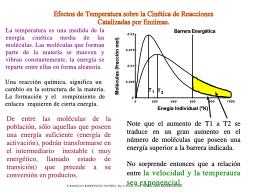
Efecto de T sobre la RXN química
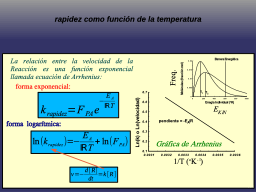
La Ec. de Arhenius
Slide 125
El valor de Q10
La teoría de Eyring-Polanyi
La formulación de Kramer
Efectos sobre la estabilidad ¿existe T óptima?
Regulación de las enzimas
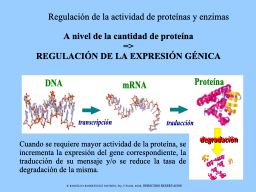
Niveles de regulación
Nivel de la expresión génica
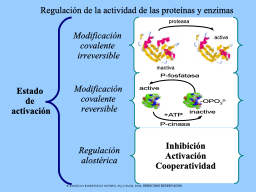
Nivel del estado de activación
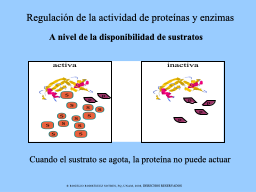
Disponibilidad de sustrato
Modulación por ligandos
Unión de ligandos a una proteína
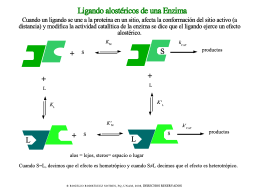
Concepto de alosterísmo
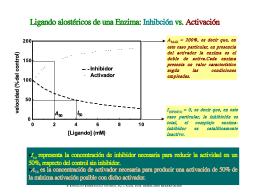
Tipos de efectos evocados por ligandos
Constantes de disociación Ki y Ka
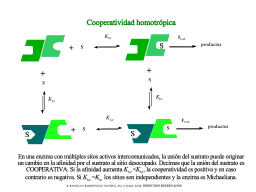
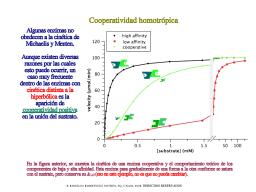
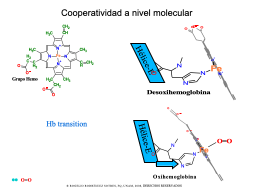
Unión cooperativa
Saturación sigmoide
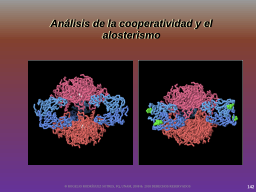
Análisis de la cooperatividad y el alosterismo
Pragmatismo. Modleo de Hill
Descripción operativa. Ecuación de Adair
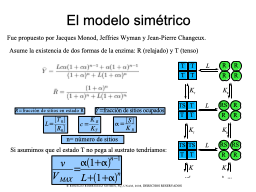
El modelo simétrico MWC
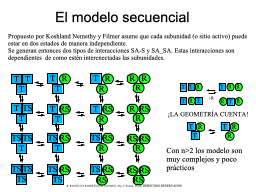
El modelo secuencial KNF
Un breve vistazo a las bases moleculares del alosterismo
Análisis de la inhibición
Moduladores y constantes de disociación
Casos de inhibición posibles
Casos de activación posibles
Ejemplo del análisis de inhibición S.R.T.
Parámetros APARENTES
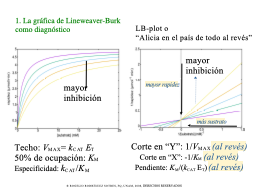
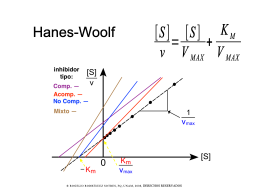
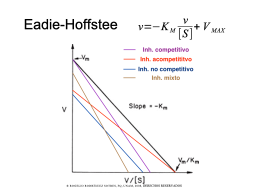
Diagnótico mediante dobles recíprocos
Inhibición Competitiva
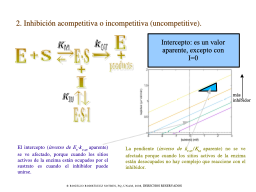
inhibición acompetitiva
Slide 157
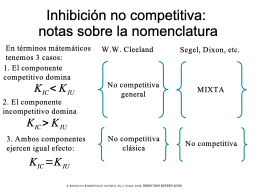
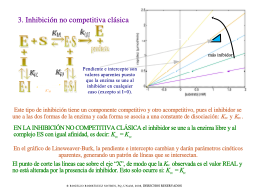
No competitiva clásica
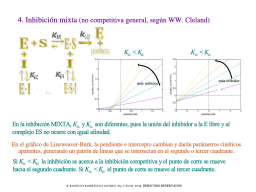
Inhibición Mixta
Parámetros por ajuste global
Slide 161
Slide 162
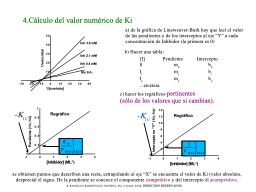
Regráficos
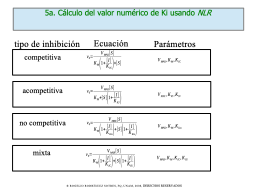
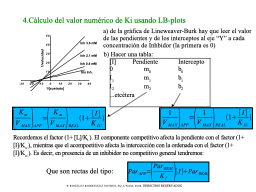
El valor de Kic y Kiu
Inactivación covalente
inactivantes
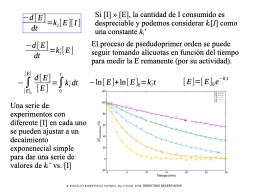
Inactivación pseudoprimer order
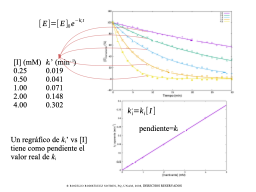
El regráfico lineal da la constate
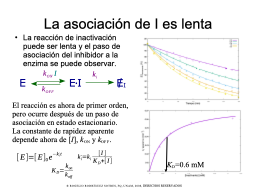
La asociación de I es lenta
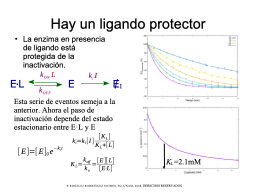
Hay un ligando protector
Ajuste de los regráficos
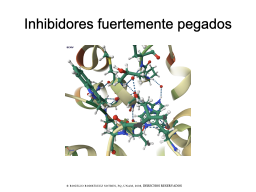
Inhibidores fuertemente unidos
Como describirlos
|
Author: Rogelio Rodríguez Sotres Email: sotres arroba unam mx Homepage: http://sitios.quimica.unam.mx/departamento/proteinas/ Further information: 


































![Una RXN enzimática: variando [S]](thumb74.png)
![¿Qué pasa si varío [S] con [E] constante?](thumb75.png)
![La rapidez si depende de [S]](thumb76.png)
![Una RXN enzimática: variación en [E]](thumb77.png)

![Caso extremo con [S] >> Km](thumb88.png)
![Caso extremo con [S] << Km](thumb89.png)


![La grafica 1/V vs. 1/[S] e incertidumbre](thumb96.png)




![Relación entre kcat y [E·S]](thumb108.png)
![Relación entre V/K y [E]libre](thumb109.png)






![Efectos sobre [E]libre y [ES]](thumb120.png)






















|